图片来源:摄图网
近年来,国家层面不断出台相关政策,加速创新药的审批和上市流程,这一举措极大地促进了医药行业的发展,加快了新药研发和上市的速度,为患者提供了更多更好的治疗选择。近日,港股上市公司康方生物宣布,国家药品监督管理局已批准公司自主研发的全球首创双特异性抗体新药依达方(依沃西注射液,PD -1 / VEGF )的新药上市申请,适应症为联合化疗用于治疗经表皮生长因子受体("EGFR")酪氨酸激霉抑制剂("TKI")治疗后进展的EGFR突变的局部晚期或转移性非鳞状非小细胞肺癌。
康方生物是广东近年来积极打造生物医药创新高地的产业代表,而依沃西单抗注射液的产品持有人为康方赛诺医药有限公司,为康方生物旗下子公司。至此,广东造创新药再添重磅新军。
据悉,依沃西单抗注射液是全球第一个获批上市的肿瘤免疫+抗血管生成机制的双特异性抗体新药,也是中国第二个获批上市的自主研发的双特异性抗体新药,有望为肺癌患者提供新的治疗选择。
截至目前,康方生物已自主开发50个以上用于治疗肿瘤、自身免疫、炎症、代谢疾病等重大疾病的创新候选药物,已有19个新药在全球开展了超过120多项临床研究,包括依沃西单抗在内的多个创新药获得国家药监局批准上市。
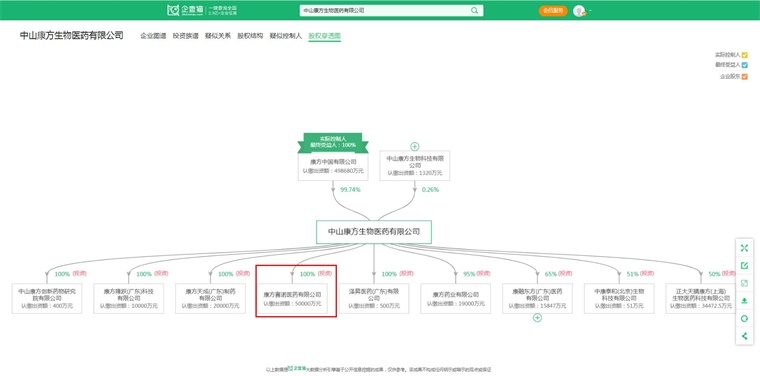
康方生物全称中山康方生物医药有限公司。据企查猫显示,中山康方生物医药有限公司成立于2012年03月19日,注册资本500,000万人民币,法定代表人XIA YU,公司经营范围包括:许可项目:药品生产;药品批发;药品进出口等。
据企查猫股权穿刺图显示,中山康方生物医药有限公司对外投资企业共有9家,其中就包括康方赛诺医药有限公司,由康方生物100%控股投资。

从康方生物的依沃西单抗注射液获批上市回看创新药行业发展情况:
——中国创新药行业处在高速发展期
中国创新药行业经历了从初期起步到如今不断崭露头角的漫长发展过程,政府支持、产业投入和国际合作的推动将进一步促进该行业的快速成长。

——中国创新药申报与审评情况
根据2022年CDE(国家药品监督管理局药品审评中心)药审报告数据,2022年1类创新药申请946个品种(受理号1727个),其中化药申请452个品种(受理号1036个),同比减少12.0%,包含IND(新药临床研究审批)申请436个品种,NDA(新药申报注册上市)申请16个品种;中药申请42个品种(受理号48个),同比减少19.2%,包含IND申请33个品种,NDA申请9个品种;生物制品申请452个品种(受理号643个),同比增长8.3%,包含IND申请441个品种,NDA申请13个品种。
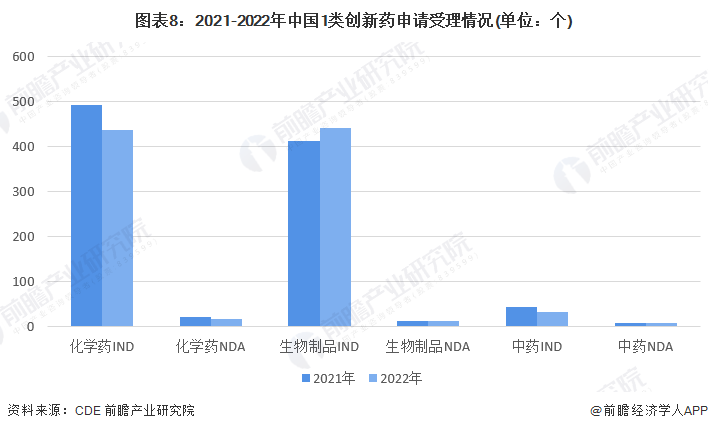
根据2022年CDE药审报告数据,2022年1类创新药完成审评994个品种(受理号1760个),其中,化药完成审评488个品种(受理号1019个),其中,IND申请476个品种,NDA申请14个品种;中药完成审评共46个品种,IND申请39个品种,NDA申请7个品种;生物制品完成审评460个品种(受理号571个),同比增长17.9%,其中,IND申请452个品种,NDA申请8个品种。

从治疗领域来看,2022年1类创新药获批上市共21个品种,适应症包含抗肿瘤领域、心血管系统、消化道及代谢等。

——中国创新药市场规模
目前,创新药市场规模在中国医药市场中占主导地位。同时,得益于利好创新药物的政策、医疗保险的动态调整、研发开支增加等原因,中国创新药市场规模的增长速度将高于仿制药市场。2021年,中国创新药市场规模为9470亿元;根据Frost & Sullivan测算,2022年市场规模突破万亿元大关,约为10234亿元。
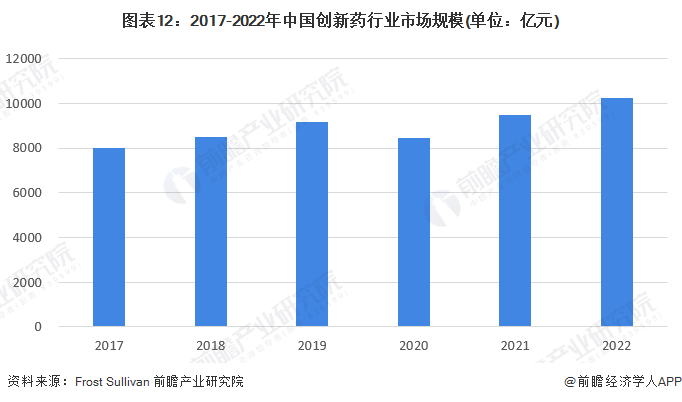
产业研究院分析认为,政府的政策支持和资金投入,以及科研实力的不断提升,为创新药研发提供了坚实基础。巨大的市场潜力、国际竞争力的增强和技术突破,将推动创新药在中国及全球市场的崭露头角。国际合作的拓展也将为行业带来更多机遇。到2028年,中国创新药行业市场规模或将达到17916亿元,市场前景广阔。
千际投行认为,中国创新药行业的未来充满希望,通过持续的技术革新和适应全球市场的变化,有望在全球医药行业中占据更重要的地位。首先,政策支持是推动中国创新药行业发展的重要驱动力。经济层面,中国的中产阶级不断壮大,人们对健康和生活质量的要求日益提高,直接推动了对高效、安全创新药的需求。社会环境方面,中国正在迈入深度老龄化社会,老年人口的增多将带来对慢性疾病治疗药物的巨大需求。此外,技术进步是支撑中国创新药行业持续发展的基石,人工智能、大数据、云计算等现代信息技术的应用正在极大地改变药物研发的模式和过程。
经济学人APP资讯组
看完觉得写得好的,不防打赏一元,以支持蓝海情报网揭秘更多好的项目。